| 时间:2026-03-06 |
脂肪为何失控疯长?骨骼又为何异常增生?同一种基因突变,如何导演出一场脂肪与骨骼的“双重疯长”大戏?答案,或许就藏在组蛋白的乳酰化修饰与P300蛋白的棕榈酰化之间。本期,京房生物将带您解读两篇合作客户发表的高水平研究论文,看看他们是如何利用ChIP-Seq、CUT&Tag、ATAC-Seq等核心技术,揭开罕见病FIL背后的表观遗传“黑手”。
这两篇论文分别发表在《Stem Cell Research & Therapy》(IF: 7.3)和 《Advanced Science》(IF: 14.1)上,可以说是在干细胞研究和交叉科学领域都引起了不小的关注。面部浸润性脂肪瘤病(Facial Infiltrating Lipomatosis,FIL)的特点是面部脂肪和骨骼“不受控制”地过度生长,严重影响了患者的容貌和生活质量。那么,它的背后究竟藏着怎样的“黑手”呢?让我们一探究竟。
第一幕:乳酰化修饰的“正反馈”狂飙 —— 解读《H3K18 lactylation-hexokinase 2 positive feedback loop promotes osteogenesis of ASPCs in facial infiltrating lipomatosis》
我们知道,FIL的“病根”很大程度上源于一个叫PIK3CA的基因发生了突变。这个突变导致细胞内的代谢异常,产生了更多的乳酸。而乳酸,并不仅仅是一个代谢废物,它还能引发一种叫做“组蛋白乳酰化”的崭新表观遗传修饰。
1. “乳酰化”登场:H3K18la是“罪魁祸首”
研究者们首先发现,在FIL患者的脂肪干细胞(ASPCs)中,乳酰化水平异常增高,尤其是第18位赖氨酸残基上的乳酰化(H3K18la)最为显著(图1G-J)。Western Blot结果显示,与正常对照(CON)相比,FIL患者的脂肪干细胞(FIL-ASPCs)中H3K18la水平显著升高。
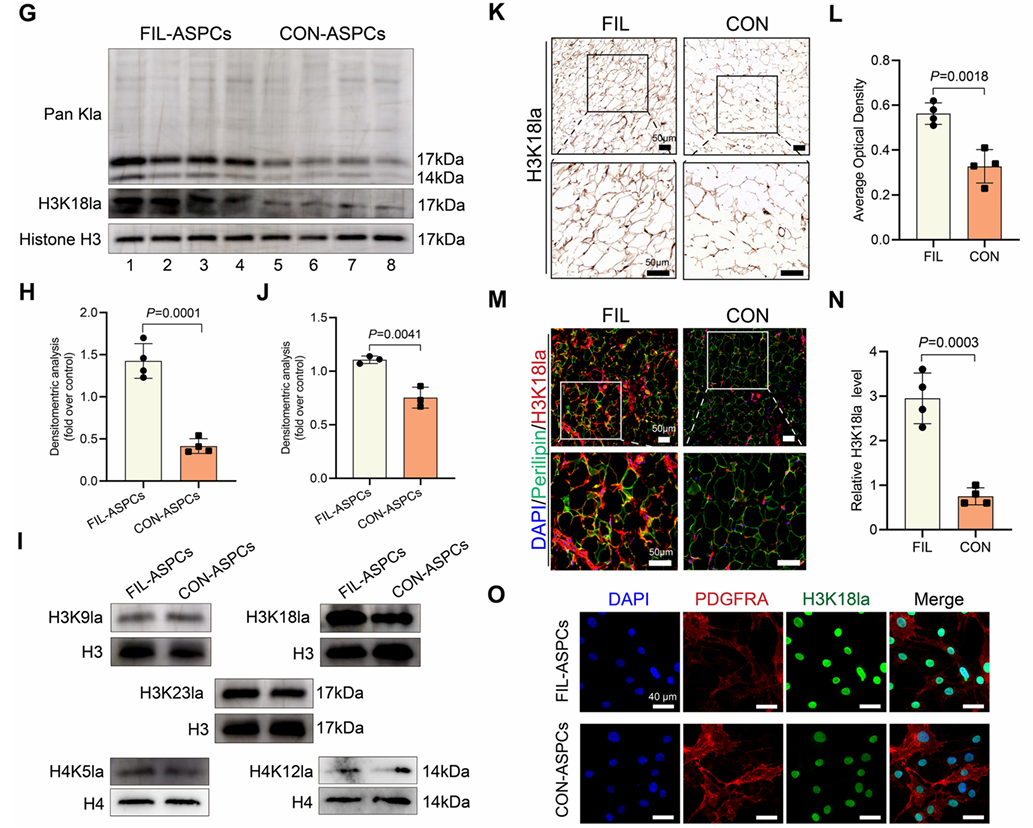
图1. FIL 脂肪组织和 FIL-ASPCs 中的乳酸化水平增加(仅展示部分结果)
2. 京脉生物核心技术登场:CUT&Tag锁定下游靶基因
那么,H3K18la的升高是如何导致骨骼过度生长的呢?为了回答这个问题,研究团队使用了我们京脉生物的拳头技术之一——CUT&Tag 进行全基因组范围的靶点鉴定。通过CUT&Tag测序,他们发现H3K18la在FIL-ASPCs中,特别富集在一系列与成骨分化相关的基因启动子区域,比如 RUNX2、ALPL、BMP7 等(图4G-L)。这说明,H3K18la就像一个“开关”,直接“坐镇”在成骨基因的“指挥部”,开启了它们的转录,从而促进了ASPCs向骨细胞分化,导致了骨组织的异常增生。
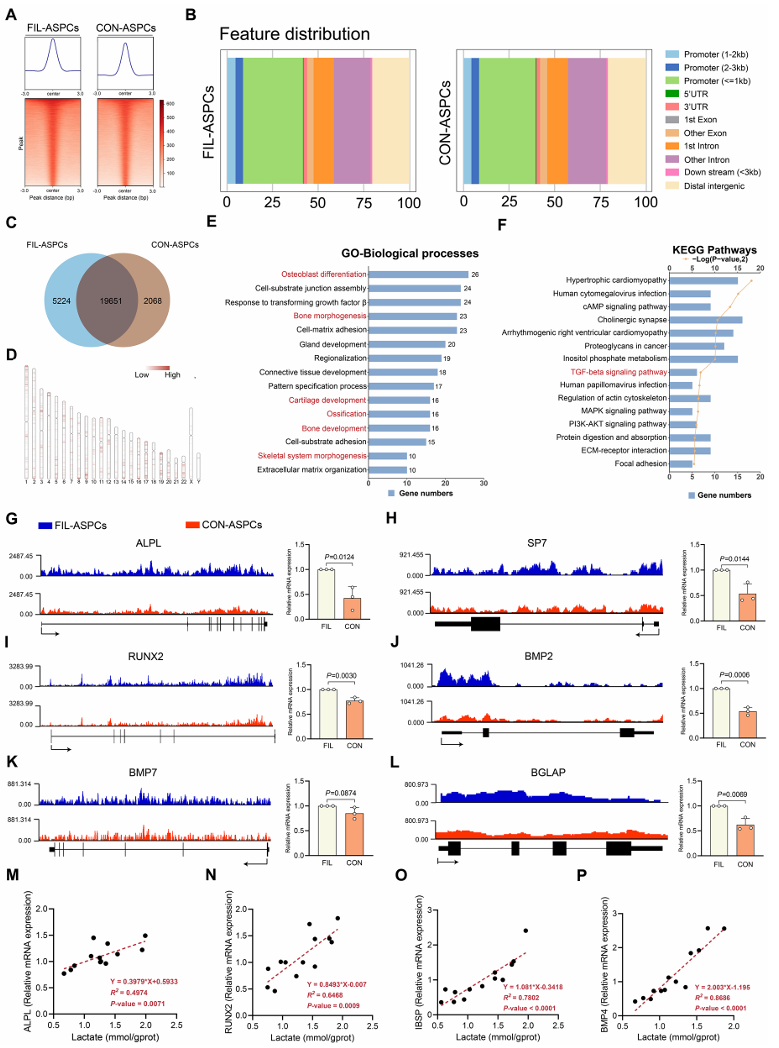
图4 通过全基因组CUT&Tag分析鉴定H3K18乳酸化的潜在下游靶点(仅展示部分结果)
更精彩的是,他们发现H3K18la还能直接上调一个糖酵解关键酶——己糖激酶2(HK2) 的表达(图6A-D)。HK2的上调会进一步增强糖酵解,产生更多的乳酸,而更多的乳酸又会反过来促进H3K18la的形成。一个可怕的 “乳酸-H3K18la-HK2”正反馈环路就此形成,像滚雪球一样,不断放大成骨效应(图6L)。
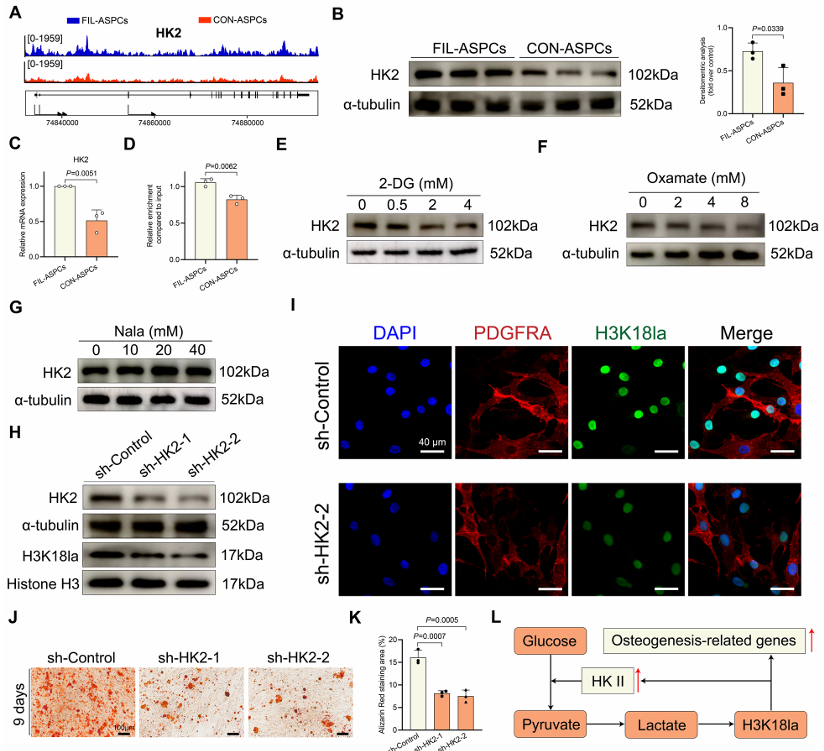
图6 由H3K18la和HK2驱动的反馈环促进了成骨作用(仅展示部分结果)
这项研究将代谢重编程与表观遗传修饰完美地联系起来。如果没有 CUT&Tag 这种高分辨率、低背景的染色质靶向测序技术,我们很难精准地定位到H3K18la在全基因组范围内的“落脚点”,更无法揭示其与HK2和成骨基因之间的直接调控关系。这正是京脉生物所擅长的——用最前沿的技术,帮您看清表观调控的每一个细节。
第二幕:棕榈酰化与相分离的“双重奏” —— 解读《PIK3CA Mutations Downregulate PPT1 to Promote Adipogenesis by Suppressing P300 Depalmitoylation and Phase Separation》
如果说第一篇论文讲的是“骨骼疯长”的故事,那么这第二篇则揭示了FIL中“脂肪堆积”的另一面。同样是PIK3CA突变,这次的主角变成了一个叫PPT1的去棕榈酰化酶。
1. 单细胞测序锁定关键基因PPT1
研究者首先利用单细胞测序技术,对FIL患者的脂肪组织进行了分析,发现了一个关键的基因——PPT1,它在FIL患者的脂肪干细胞(ASPCs)中表达显著下调(图1A-C)。
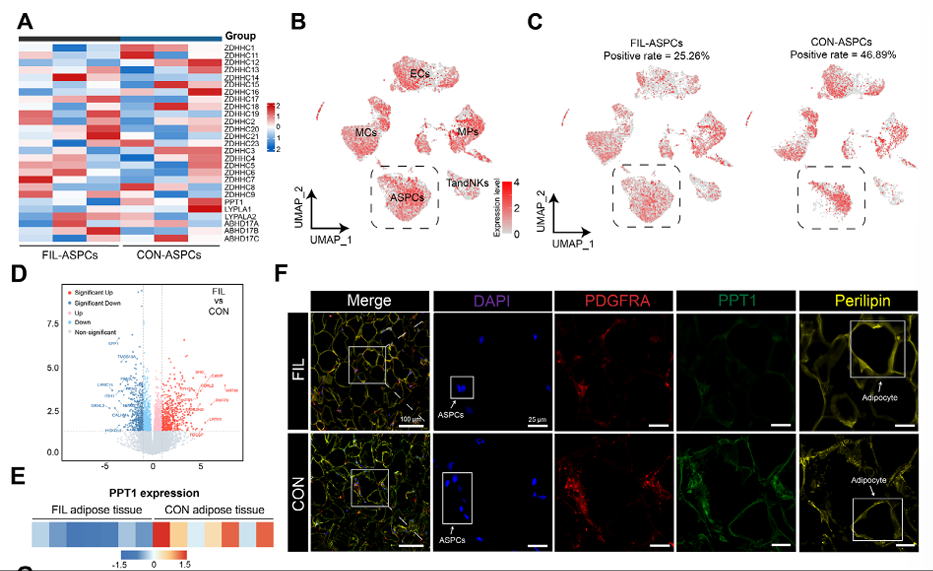
图1 FIL中PPT1的下调与其严重程度相关(仅展示部分结果)
2. 一条清晰的信号通路:从PIK3CA到PPT1
他们进一步发现,突变的PIK3CA通过经典的PI3K-AKT通路,激活了转录因子c-JUN。而c-JUN直接结合到PPT1基因的启动子上,阻止了PPT1的转录,导致了PPT1蛋白的减少(图2L-O)。为了验证c-JUN与PPT1启动子的结合,研究者们使用了染色质免疫沉淀-定量PCR(ChIP-qPCR)技术,这正是京脉生物提供的常规但至关重要的验证手段。
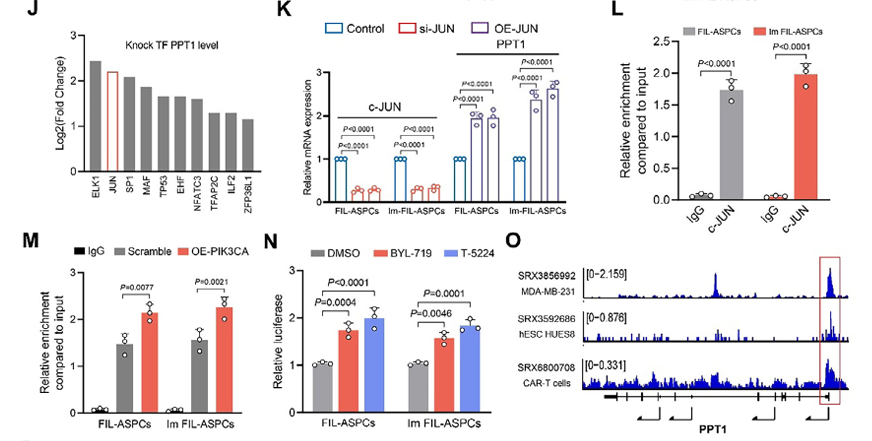
图2 PIK3CA 突变通过c-JUN抑制PPT1表达(仅展示部分结果)
3. PPT1缺失,P300“黑化”
那么PPT1减少后会发生什么呢?PPT1的功能是去除蛋白质的棕榈酰化修饰。通过免疫沉淀-质谱(IP-MS)分析,他们找到了PPT1的一个互作蛋白——大名鼎鼎的转录共激活因子 P300。P300是细胞内一个关键的“表观调控枢纽”,负责给组蛋白加上乙酰化修饰(如H3K27ac、H3K9ac),从而激活基因转录。研究者们发现,PPT1的减少导致P300蛋白上的一个关键位点(C1176)的棕榈酰化水平异常升高(图5H-J)。这种异常的修饰,一方面让P300“逃避”了通过分子伴侣HSC70介导的溶酶体降解途径,大大增加蛋白稳定性(图6D-E);另一方面,它还抑制了P300的液-液相分离能力(图8G-H)。
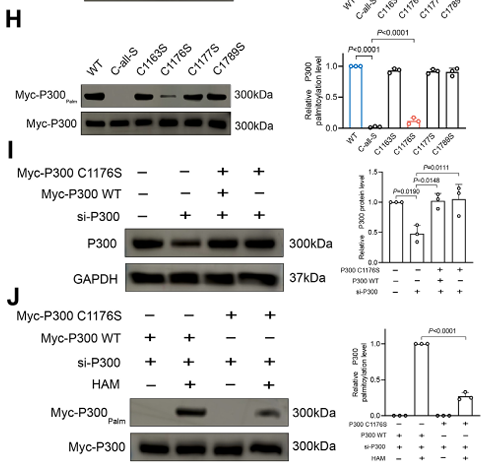
图5 PPT1调节了FIL-ASPCs中P300的棕榈酰化(仅展示部分结果)
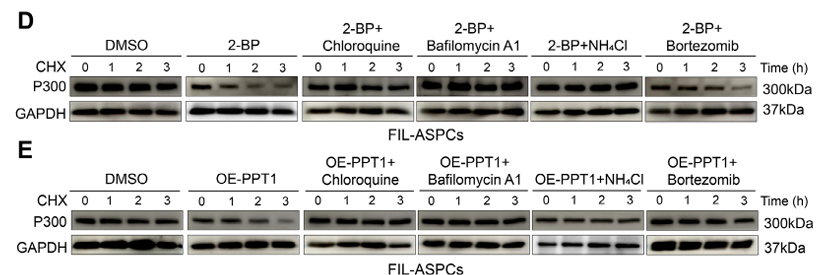
图6 PPT1通过对Cys1176的去棕榈酰化促进了P300的降解(仅展示部分结果)
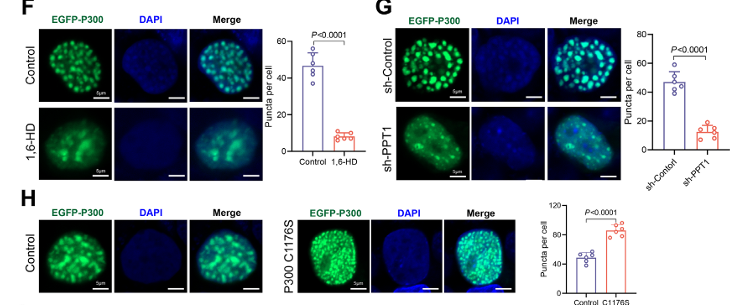
图8 P300棕榈酰化抑制相分离(仅展示部分结果)
4. 京脉生物多组学联合分析:P300如何开启成脂“总开关”
稳定且“不”的P300,其组蛋白乙酰转移酶活性得以保持。研究者接着通过RNA测序(RNA-seq) 和 ATAC测序(ATAC-seq) 全面评估了P300的功能。RNA-seq 发现,在P300被敲低后,大量与脂肪生成相关的基因,如 PPARγ、CEBPA、FABP4 等,表达显著下调(图7A-E)。ATAC-seq 则揭示,P300的敲低导致这些成脂基因的启动子区域染色质开放性显著下降(图7J, M-N)。这意味着,P300像一个“开路先锋”,它维持着染色质的开放状态,让转录机器能够顺利到达目标基因,启动成脂程序。
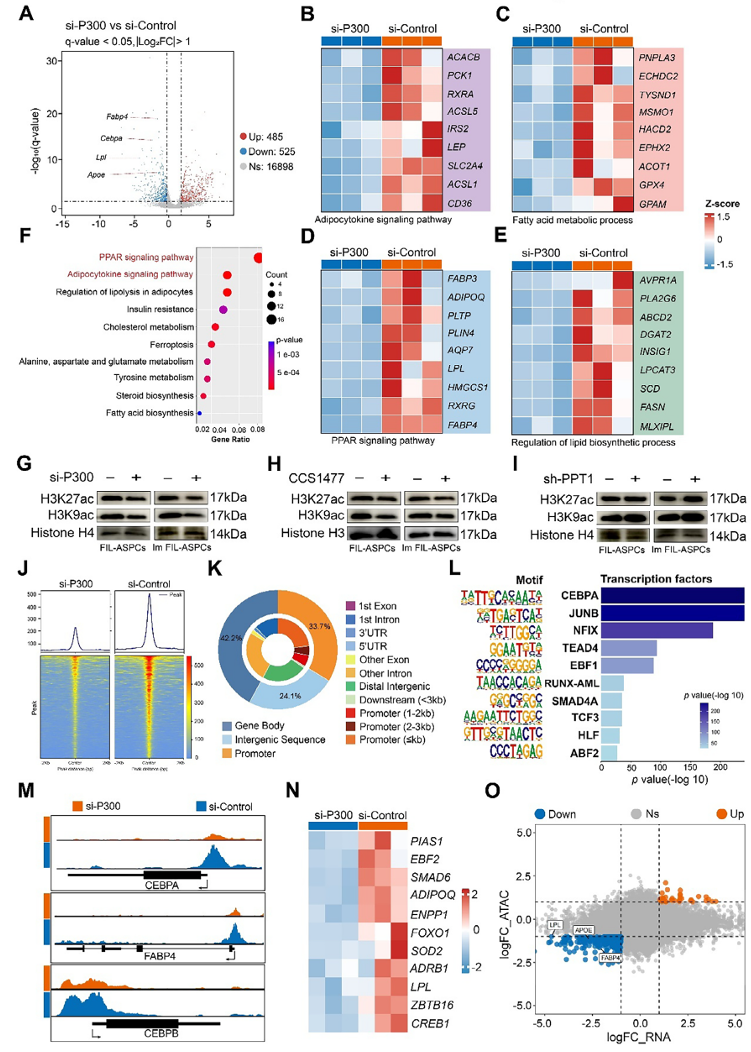
图7 P300通过转录重新编程促进脂肪生成
最终,研究者勾画出了一条完整的通路:PIK3CA突变→c-JUN激活→PPT1转录抑制→P300棕榈酰化升高→P300稳定性增加&相分离能力下降→染色质开放和组蛋白乙酰化水平维持→成脂基因转录激活→脂肪过度增生。
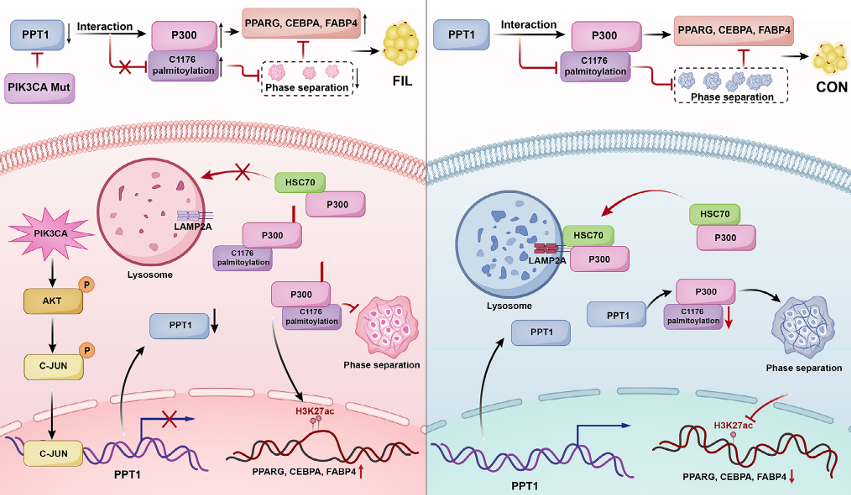
图10 PPT1介导的P300去棕榈酰化通过促进相分离凝聚体的形成抑制脂肪生成
这项研究的格局非常宏大,从最初的单细胞测序发现线索,到ChIP-qPCR验证调控机制,再到IP-MS钓取互作蛋白,最后用RNA-seq和ATAC-seq阐明功能,形成了一个完美的闭环。这也正是京脉生物所倡导的研究范式:综合运用多种前沿技术,从多维度、多层次地解析复杂的生物学问题。无论您是关注组蛋白修饰、染色质开放性,还是转录调控网络,京脉生物都能为您提供高质量的文库构建、测序和专业的生信分析服务,助您的科研之路一臂之力。
第三幕:结语
两篇论文,一个聚焦“乳酰化”,一个聚焦“棕榈酰化-相分离”,虽然机制不同,但都共同指向了FIL中“脂肪-骨骼”双重病变的复杂性,也共同证明了表观遗传调控在这一过程中的核心地位。
作为技术提供方,京脉生物很荣幸能见证并参与这样高水平的研究。我们相信,随着 ChIP-Seq、CUT&Tag、ATAC-Seq、单细胞测序等技术的不断发展和普及,将会有越来越多疾病的“表观密码”被破译,为患者带来新的希望。
如果您也对表观遗传学、基因组学或衰老研究(我们的甲基化时钟技术也相当成熟哦!)感兴趣,欢迎随时联系我们。京脉生物,期待成为您探索生命奥秘路上的最佳伙伴!